લિસિન અને એલ-લિસિન વચ્ચે તફાવત. લિસિન વિ. એલ-લિસિન
કી તફાવત - લિસિન વિ એલ-લિસીન
લિસિન અને એલ-લિસિન એ બંને પ્રકારના એમિનો એસિડ છે, છતાં ભૌતિક ગુણધર્મો વહેંચતા, ત્યાં છે તેમની વચ્ચે કેટલાક તફાવત. લિસિન અને એલ-લિસિન વચ્ચેનું મુખ્ય તફાવત એ પ્લેન ધ્રુવીકૃત પ્રકાશને ફેરવવાની ક્ષમતા છે. લિસિન એક જીવવિજ્ઞાન સક્રિય છે, જે કુદરતી રીતે આવશ્યક α-amino acid છે. Chiral કાર્બન અણુ આસપાસ બે અલગ અલગ enantiomers રચના કરવાની શક્યતા કારણે તે બે isomeric સ્વરૂપો થઇ શકે છે. આને L- અને D- સ્વરૂપો તરીકે ઓળખવામાં આવે છે, ડાબા-હાથે અને જમણા હાથની ગોઠવણી માટે સમાન. આ એલ અને ડી સ્વરૂપો ઓપ્ટિકલ સક્રિય હોવાનું કહેવાય છે અને અલગ અલગ અર્થમાં પ્લેન ધ્રુવીકરણિત પ્રકાશને ફેરવો; ઘડિયાળની દિશામાં અથવા એન્ટિકૉકવૉલ જો પ્રકાશમાં લાઈસિન એન્ટિકૉકવૉલિસ ફરે છે, તો પછી પ્રકાશ હવાની અણીએ દર્શાવે છે, અને તેને એલ-લિસિન તરીકે ઓળખવામાં આવે છે. જો કે, તે અહીં કાળજીપૂર્વક નોંધેલું હોવું જોઈએ કે ડી- અને એલ-લેબલિંગ ઇસ્મોમર્સ ડી-અને એલ-લેબલિંગ જેવી નથી.
લિસિન શું છે?
લિસિન એ એક આવશ્યક એમિનો એસિડ છે જે આપણા શરીરમાં સંશ્લેષણિત નથી અને તેને નિયમિત આહાર દ્વારા પૂરી પાડવામાં આવે છે. એના પરિણામ રૂપે, lysine માનવ માટે એક આવશ્યક એમિનો એસિડ છે. રાસાયણિક સૂત્ર NH 2 - (CH 2) સાથે એમોન (-NH 2 ) અને કાર્બોક્ઝિલિક એસિડ (-COOH) વિધેયાત્મક જૂથો સાથે બનેલી એક જૈવિક મહત્વપૂર્ણ કાર્બનિક સંયોજન છે. >) 4 -CH (NH 2 ) - કોહ. લિસિનના ચાવીરૂપ ઘટકો કાર્બન, હાઇડ્રોજન, ઓક્સિજન અને નાઇટ્રોજન છે. બાયોકેમિસ્ટ્રીમાં, પ્રથમ (આલ્ફા) કાર્બન પરમાણુ સાથે જોડાયેલા એમાઈન અને કાર્બોક્સિલેક એસિડ જૂથો એમિનો એસિડ્સને α-amino acids તરીકે ઓળખવામાં આવે છે. આમ લૅસિનને α-amino acids તરીકે પણ ગણવામાં આવે છે. લસિનનું માળખું આકૃતિ 1 માં આપવામાં આવ્યું છે. આકૃતિ 1: લૅસિનનું મોલેક્યુલર માળખું (* કાર્બન પરમાણુ ચાઇરલ અથવા અસમપ્રમાણિત કાર્બન અણુ છે અને આલ્ફા-કાર્બન અણુનું પણ પ્રતિનિધિત્વ કરે છે)
લિસિન મૂળભૂત સ્વભાવ છે કારણ કે તેમાં બે મૂળ એમિનો જૂથો અને એક અમ્લીય કાર્બોક્ઝિલિક એસિડ જૂથ. આથી, તે બે એમિનો જૂથોની હાજરીને કારણે વ્યાપક હાઇડ્રોજન બંધનની રચના કરે છે.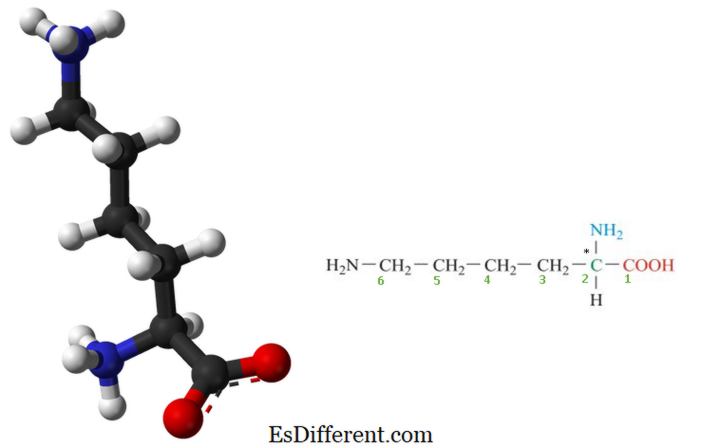
લૅસિનના સારા સ્ત્રોતો
પ્રોટીન સમૃદ્ધ પ્રાણી સ્ત્રોતો છે જેમ કે ઇંડા, લાલ માંસ, ઘેટાં, ડુક્કર, અને મરઘાં, પનીર અને અમુક માછલી (જેમ કે કૉડ અને સારડીનજ). લિસિન પણ પ્લાન્ટ પ્રોટીનથી સમૃદ્ધ છે સોયા, કઠોળ અને વટાણા જેવી. જો કે, તે મોટાભાગના અનાજના અનાજમાં એમિનો એસિડ મર્યાદિત છે પરંતુ તે મોટા ભાગની કઠોળ અને કઠોળમાં વિપુલ પ્રમાણમાં છે.
nd
કાર્બનની આસપાસ ચાર જુદા જુદા જૂથો છે, અને તે અસમપ્રમાણ માળખું છે.આ અસમપ્રમાણતાવાળા અથવા ચીરલ કાર્બન અણુની હાજરીને કારણે, લિસિન ઓપ્ટિકિકલી સક્રિય એમિનો એસિડ છે. આ રીતે, લિસિન એવા સ્ટીરીયોઇસોમર્સ બનાવી શકે છે, જે આણ્વિક પરમાણુઓ ધરાવે છે જે સમાન પરમાણુ સૂત્ર ધરાવે છે, પરંતુ અવકાશમાં તેમના અણુઓના ત્રિ-પરિમાણીય દિશામાં અલગ પડે છે. એન્એન્ટીયોમર્સ બે સ્ટીરીયોઇઝર્સ છે જે પ્રતિબિંબ દ્વારા એકબીજા સાથે સંબંધિત છે અથવા તે એકબીજાના દર્પણ છબીઓ છે જે બિન-સુપરિપોઝૉવબલ છે. Lysine L- અને D- તરીકે ઓળખાય છે બે enantiomeric સ્વરૂપો માં ઉપલબ્ધ છે અને lysine ના enantiomers 2 આકૃતિ માં આપવામાં આવે છે. આકૃતિ 2: lysine એમિનો એસિડ ઓફ Enantiomers. COOH, H, R અને NH2 જૂથો ઘડિયાળની દિશામાં સી અણુની આસપાસ ગોઠવાય છે, એન્એન્ટીયોમરને એલ ફોર્મ અને ડી-ફોર્મ તરીકે ઓળખવામાં આવે છે. L- અને D- માત્ર કાર્બન અણુની આસપાસની અવકાશી ગોઠવણીનો ઉલ્લેખ કરે છે અને ઓપ્ટિકલ પ્રવૃત્તિનો ઉલ્લેખ કરતા નથી. જ્યારે ચિકર અણુના એલ- અને ડી-સ્વરૂપો વિવિધ દિશામાં ધ્રુવીકૃત પ્રકાશના વિમાનને ફેરવતા હોય છે, ત્યારે કેટલાક એલ-સ્વરૂપો (અથવા ડી-સ્વરૂપો) પ્રકાશને ડાબે (લેવો અથવા એલ-ફોર્મ) અને કેટલાકને જમણે ફેરવો (ડીક્સ્ટ્રો અથવા ડી-ફોર્મ). એલ- અને ડી-ફોર્સ ઓપ્ટિકલ ઇસ્મોમર્સ કહેવાય છે. એલ-લિસીન અને ડી-લિસિન એ એકબીજાના એન્ટિએનોમિમર્સ સમાન ભૌતિક ગુણધર્મો ધરાવે છે, સિવાય કે તે દિશા સિવાય તે ધ્રુવીકરણવાળા પ્રકાશને ફેરવશે. તેઓ બિન-સુપરિમ્પોઝબલ મિરર ઇમેજ સંબંધ ધરાવે છે. જોકે, ડી અને એલ ના નામકરણમાં લિસિન સહિત એમિનો એસિડ્સમાં સામાન્ય નથી. તેઓ પ્લેન-ધ્રુવીકૃત પ્રકાશને સમાન તીવ્રતામાં ફેરવતા હોય છે પરંતુ જુદી જુદી દિશામાં. લિસિનના ડી અને એલ આઇસોમર જે ઘડિયાળની દિશામાં દિશામાં ઉડ્ડયન કરેલા પ્રકાશને ફેરવે છે તેને ડેક્ષ્ટ્રોરોટેટરી અથવા

ડી-લિસિન
તરીકે કહેવામાં આવે છે અને જે એન્ટીકલોકિસિવ દિશામાં પ્લેન ધ્રુવીકૃત પ્રકાશને ફરે છે તેને લેવરોટોરેટરી કહેવાય છે અથવા એલ-લિસિન (આકૃતિ 2). એલ-લિસિન એ લિસિનનું સૌથી વધુ ઉપલબ્ધ સ્થિર સ્વરૂપ
છે. ડી-લિસિન એ લિસિનનું સિન્થેટિક સ્વરૂપ છે અને તેને રેસિમાઇઝેશન દ્વારા એલ-લિસિનથી સંશ્લેષણ કરી શકાય છે. તેનો ઉપયોગ પોલિ-ડી-લસિનની પ્રક્રિયામાં થાય છે, જેનો ઉપયોગ સેલ જોડાણ વધારવા માટે કોટિંગ સામગ્રી તરીકે થાય છે. એલ-લિસિન માનવ શરીરમાં મહત્વપૂર્ણ ભૂમિકા ભજવે છે, કેલ્શિયમ શોષણ, સ્નાયુ પ્રોટીન વિકાસ, અને હોર્મોન્સ, એન્ઝાઇમ અને એન્ટિબોડીઝનું સંશ્લેષણ. ઔપચારીક રીતે, એલ-લિસીનનું ઉત્પાદન કોરીએબેક્ટેરિયમ ગ્લુટામેકિયમ નો ઉપયોગ કરીને માઇક્રોબાયલ આથોની પ્રક્રિયા દ્વારા કરવામાં આવે છે. લિસિન અને એલ-લિસિન વચ્ચે શું તફાવત છે? લિસિન અને એલ-લિસિન પાસે સમાન ભૌતિક ગુણધર્મ હોય છે, સિવાય કે તે દિશા સિવાય તે ધ્રુવીકરણવાળા પ્રકાશને ફેરવે છે. પરિણામે, એલ-લિસિનમાં નોંધપાત્ર વિવિધ જૈવિક અસરો અને વિધેયાત્મક ગુણધર્મો હોઈ શકે છે. જો કે, આ જૈવિક અસરો અને વિધેયાત્મક ગુણધર્મોને અલગ પાડવા માટે ખૂબ જ મર્યાદિત સંશોધન કરવામાં આવ્યું છે. આમાંના કેટલાક તફાવતો શામેલ હોઈ શકે છે,
સ્વાદ
એલ-લિસિન:
એમિનો એસિડનું L- સ્વરૂપો સ્વાદવિહીન હોય છે.
ડી-લિસિન: એમિનો ઍસિડના ડી-સ્વરૂપો મીઠાંનો સ્વાદ લેતા હોય છે.
આથી એલ-લિસિન લસિન કરતા ઓછી / કોઈ મીઠું હોઈ શકે છે વિપુલતા
એલ-લિસિન:
એલ-લિસિન સહિતના એમિનો એસિડના સ્વ-સ્વરૂપો સ્વભાવમાં સૌથી વધુ સમૃદ્ધ સ્વરૂપ છે.ઉદાહરણ તરીકે, સામાન્ય રીતે પ્રોટીનમાં જોવા મળેલ ઓગણીન એલ-એમિનો એસિડ્સમાંથી નવ ડેક્ષ્ટ્રોરોટેટરી છે અને બાકીના લેવોટોરેટરી છે.
ડી-લિસિન: પ્રાયોગિક ધોરણે જોવા મળતી એમિનો એસિડના ડી-ફોર્મ ખૂબ જ ભાગ્યે જ જોવા મળે છે.
સંદર્ભો: સોલોમોન્સ, ટી. ડબ્લ્યુ. ગ્રેહામ, અને ગ્રેગ બી ફ્રીહલે (2004). કાર્બનિક કેમિસ્ટ્રી (8 મી
ઇડી) હોબોકેન: જ્હોન વિલી એન્ડ સન્સ, ઇન્ક. એવરહાર્ડસ, એ. (1984). સ્ટિરોકેમિસ્ટ્રી, ફાર્માકોકિનેટિક્સ અને ક્લિનિકલ ફાર્માકોલોજીમાં વ્યવહારુ નોનસેન્સનો એક આધાર, યુરોપિયન જર્નલ ઓફ ક્લિનિકલ ફાર્માકોલોજી, 26, 663-668. છબી સૌજન્ય: બેન મિલ્સ દ્વારા "એલ-લિસિન-મોનોકેશન-થી-હાઇડ્રોક્લોરાઇડ-ડાયહાઇડ્રેટ-xtal-3D-balls" - વિકિમીડીયા કોમન્સ દ્વારા પોતાના કામ




